EMA將啟動查廠 藥華藥估P1101明年上半年可取得藥證
鉅亨網記者李宜儒 台北
藥華藥 (6446-TW)PV 新藥 P1101 將正式進入查廠階段,藥華藥表示,接獲歐洲夥伴 AOP 通知,歐洲藥品管理局 (EMA) 指定 AGES 來台執行實地查廠,預計將查核台中廠及財團法人農業科技研究院等二處場址,公司預估,P1101 明 (2018) 年上半年可望取得藥證。

藥華藥執行長林國鐘表示,在 EMA 歐盟人體用藥委員會 (CHMP) 展開查核新藥上市申請 (MMA) 資料第 68 天後,正式進入 GMP 查廠階段,由於 EMA 要求奧利地健康及食品安全專業行政機構 (Austrian Agency for Health and Food Safety,AGES) 最晚於今年 11 月必須提出查廠報告,因此推估查廠時間將在 6-9 月間進行,若一切順利,預估於明年上半年取得藥證的目標不變。
藥華藥台中分公司營運長欒衍棟指出,EMA 對於上市藥物的品質與安全,訂有嚴謹的查廠規範,尤其蛋白質藥物的產製又較小分子化學藥物困難,對物化性質、品質保證及測試方式 (Chemistry, Manufacture and Control,CMC) 的生產稽查要求更高,因此台中廠的實地查核認證 (Pre-Approval Inspection,PAI) 是 PV 新藥繼成功完成三期臨床試驗後,邁向商業化量產上市的關鍵最後一哩。
欒衍棟表示,配合歐洲三期臨床的開展,台中廠早在 2 年前就積極準備相關查廠事宜,包括強化員工編製與訓練、延攬國內外製藥界人才、禮聘專家顧問團駐廠指導等,目前台中廠的人員編制從 2012 年建廠初期的 16 名,增加到 90 名。
藥華藥副總裁朱建超表示,今年初公司主動邀請前英國藥物與保健產品法規管理局 (MHRA) 高級審查員 Richard Funnel 進行為期一週的模擬查廠 (mock inspection),Funnel 認為台中廠無論在工廠設置、人員素質及對 GMP 概念等所有軟硬設施方面都沒有任何嚴重缺失及重要缺失,僅部分次要缺失需要進行改善。
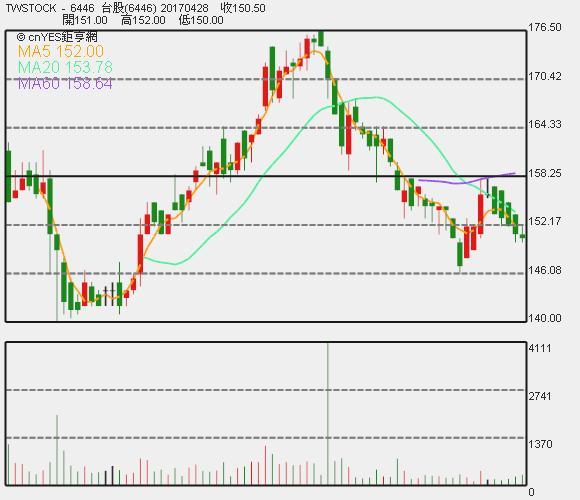
藥華藥日 K 線圖
- 權證小哥從籌碼動向看懂下半年原物料
- 掌握全球財經資訊點我下載APP
鉅亨贏指標
了解更多延伸閱讀
- 講座
- 公告
上一篇
下一篇